Diagnóstico das leucemias agudas por citometria de fluxo
Antes de continuar a leitura do texto, quero te convidar para conhecer meus cursos:
- Hematologia básica clique aqui
- Anemias clique aqui
- Onco-hematologia clique aqui
- Interpretando o hemograma clique aqui
- Curso de Hematologia (10% off) clique aqui
- Preparatório de Análises Clínicas para Residência e Concurso clique aqui
Continue agora com a sua leitura do texto. Espero que goste.
Texto por Dr. Leandro de Souza Thiago
A imunofenotipagem por citometria de fluxo (leia mais sobre a técnica aqui) revolucionou o diagnóstico das leucemias agudas, antes baseado apenas na morfologia e técnicas citoquímicas.
Quando um paciente apresenta suspeita de leucemia aguda após exame clínico e hematoscopia do sangue periférico, no qual a presença de blastos circulantes é um achado frequente, um aspirado de medula óssea faz-se necessário.
A medula óssea coletada servirá para a realização de diferentes exames complementares no laboratório especializado: mielograma, imunofenotipagem, biologia molecular, citogenética convencional e hibridização in situ com sondas fluorescentes (FISH). Tanto o mielograma quanto a imunofenotipagem são essenciais no diagnóstico rápido e preciso da leucemia aguda, sendo seus laudos liberados em geral no mesmo dia (ou no máximo no dia seguinte) do recebimento da amostra, uma vez que estas são fatais se o correto tratamento não for iniciado o mais breve possível.
Apesar de agressivas, as leucemias agudas, em particular as pediátricas, possuem uma das melhores histórias de sucesso terapêutico em oncologia, atingindo em média cerca de 80 a 85% de cura em crianças e de 90% nos pacientes pediátricos classificados como de baixo risco.
A base conceitual do diagnóstico em câncer consiste na capacidade do especialista em diferenciar casos malignos de amostras normais e casos reacionais (como infecções). Para isso, a primeira etapa do diagnóstico laboratorial (fase de triagem) tem como objetivo identificar se as células hematopoéticas possuem aberrações fenotípicas compatíveis com leucemia aguda; quantificar em termos relativos (percentual) a infiltração medular e caracterizar a linhagem celular à qual pertence o clone leucêmico (células linfóides B, células linfóides T ou células mielóides).
Para isso, utiliza-se um painel limitado de anticorpos pré-estabelecido para todos os casos, nos quais há marcadores de linhagem de células B, células T e mielóides. Além destes, inclui-se também marcadores associados à imaturidade celular, para definir se as células analisadas são células precursoras, característica biológica de todas as leucemias agudas.
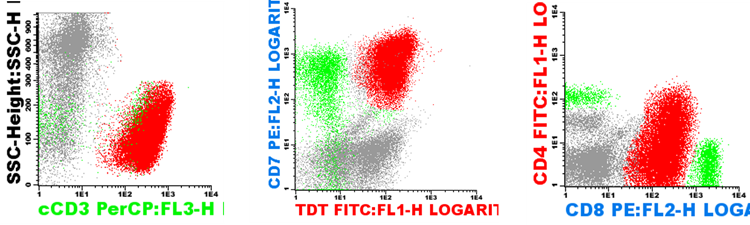
Uma vez estabelecido de que se trata de uma leucemia aguda e qual é o tipo celular maligno, segue-se para a segunda etapa, que é abrir um painel amplo pré-estabelecido de anticorpos direcionado à linhagem maligna identificada, com a intenção de subclassificar o tipo de leucemia, de acordo com o estágio de diferenciação da célula tumoral.
A classificação precisa das leucemias tem impacto clínico imediato, uma vez que ela direcionará a escolha do protocolo terapêutico inicial pelo médico assistente. Recentemente, o Grupo Brasileiro de Citometria de Fluxo (GBCFLUX) estabeleceu e publicou um protocolo de consenso para o diagnóstico imunofenotípico das leucemias agudas, com a intenção de que todos os laboratórios brasileiros trabalhem de maneira uniforme. (LINK PARA O ARTIGO).
Como são muitos os subtipos, tomemos como exemplo apenas as leucemias linfoblásticas agudas de precursores de células B (LLA-B). Em termos fenotípicos, podemos classificá-las em cinco subtipos, do mais imaturo ao subtipo com maior grau de diferenciação: Pró-B; B Comum; Pré-B; B transicional e linfoma/leucemia de Burkitt. As leucemias pró-B e de Burkitt possuem evoluções clínicas muito diferentes entre si e das demais LLA- B, o que leva a tratamentos diferenciados.
À guisa de exemplo, o linfoma/leucemia de Burkitt é altamente agressivo mas apresenta um elevado índice de cura com o tratamento específico. Caso essa entidade não seja corretamente diagnosticada, o paciente receberá o mesmo tratamento das outras LLA-B, o que levará o paciente ao óbito rapidamente por conta da evolução da doença.
Uma terceira etapa consiste em avaliar o conteúdo de DNA das células neoplásicas por citometria, usando reagentes que intercalam no DNA, como o iodeto de propídeo. A presença de aneuploidias (quantidade anormal de DNA) está fortemente associada ao prognóstico da doença.
Quando o diagnóstico final é liberado, duas ações são disparadas: A equipe clínica inicia o tratamento adequado enquanto os especialistas em biologia molecular, citogenética convencional e FISH começam a busca por alterações genéticas específicas do subtipo leucêmico previamente identificado. A identificação de alterações genéticas/moleculares específicas permitirá à equipe clínica modular o tratamento do paciente (ie. Escolher entre usar um tratamento mais agressivo ou mais leve, de acordo com o risco de cada paciente).
Não se concebe hoje em dia fazer (boa) oncohematologia clínica sem todos esses exames laboratoriais. Os avanços científicos têm permitido que cada paciente seja tratado de forma cada vez mais específica de acordo com as características de sua própria doença. O caminho em direção ao futuro é a medicina personalizada. Estamos preparados?
 Dr. Leandro de Souza Thiago é Biomédico e Doutor em Ciências Morfológicas pela UFRJ, com pós-doutorado em Imunologia pela Universidad de Salamanca (USAL, Espanha). É Tecnologista do Instituto Nacional de Câncer (INCa) e Membro Titular do Grupo Brasileiro de Citometria de Fluxo (GBCFLUX).
Dr. Leandro de Souza Thiago é Biomédico e Doutor em Ciências Morfológicas pela UFRJ, com pós-doutorado em Imunologia pela Universidad de Salamanca (USAL, Espanha). É Tecnologista do Instituto Nacional de Câncer (INCa) e Membro Titular do Grupo Brasileiro de Citometria de Fluxo (GBCFLUX).






