10 coisas que todo Biomédico deve saber sobre a Febre Amarela
Antes de continuar a leitura do texto, quero te convidar para conhecer meus cursos:
- Hematologia básica clique aqui
- Anemias clique aqui
- Onco-hematologia clique aqui
- Interpretando o hemograma clique aqui
- Curso de Hematologia (10% off) clique aqui
- Preparatório de Análises Clínicas para Residência e Concurso clique aqui
Continue agora com a sua leitura do texto. Espero que goste.
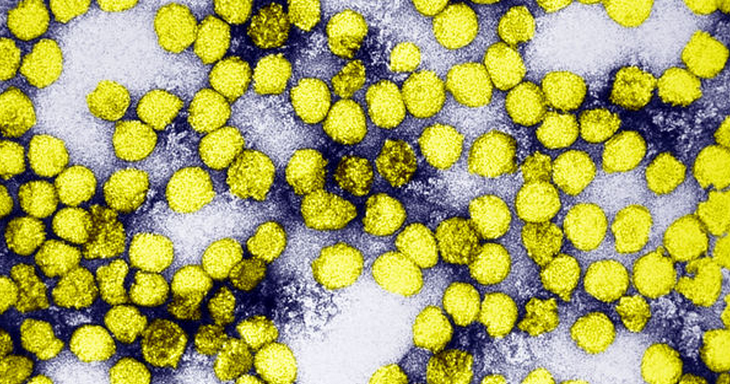
Estamos vendo ultimamente que vários estados brasileiros vêm sofrendo com surtos de Febre Amarela. Já foram notificaram ao Ministério da Saúde pelo menos 901 casos suspeitos da doença. Do total, 708 casos permanecem em investigação, 151 foram confirmados e 42 descartados. Dos 143 óbitos notificados, 54 foram confirmados, 86 ainda são investigados e 3 foram descartados.
Mas qual o agente etiológico da febre amarela e como ela é disseminada? Confira a seguir as informações mais importantes, que todo biomédico, assim como qualquer profissional da saúde, deve saber.
Você também pode escutar esse post. Dê play logo abaixo!
1. É uma Arbovirose
A febre amarela é uma infecção viral, denominada também de arbovirose. Denominam-se arbovírus (arthropod-borne viruses) os vírus cuja transmissão se dá por picada de um vetor artrópode. Entre as arboviroses que afetam o homem, 13 são causadas por vírus da família Flaviviridae, gênero Flavivirus.
2. Estirpe 17D
Apesar de a transmissão por mosquitos ter sido proposta desde 1848, a comprovação ocorreu somente em 1901, por Reed, que identificou o mosquito Aedes aegypti como vetor do vírus. Em 1927, Mahaffy e Bauer isolaram o vírus (estirpe Asibi) após inoculação do sangue de um paciente em macaco Rhesus. Dez anos depois, Theiler e Smith conseguiram atenuar a estirpe Asibi do vírus da febre amarela (YFV, yellow fever virus), por meio de passagem seriada em cultura de tecido de embrião de galinha. Essa estirpe atenuada foi denominada 17D e vem sendo empregada até hoje para imunização em seres humanos.
3. Estrutura viral
A partícula dos flavivírus mede de 40 a 60 nm de diâmetro, possui um capsídeo proteico, com simetria icosaédrica, envolvido por um envelope lipídico onde estão inseridas pequenas proteínas de membrana e espículas de natureza glicoproteica. Tem como material genético RNA de fita simples.
4. Transmissão pela fêmea do mosquito
O vírus penetra pela pele, após inoculação pelo mosquito infectado, sendo replicado, inicialmente, nos linfonodos regionais. A seguir, dissemina-se via corrente sanguínea, a outros órgãos, como fígado, rins, medula óssea, sistema nervoso central, coração, pâncreas, baço e linfonodos.

No ciclo silvestre, em áreas florestais, o vetor da febre amarela é principalmente o mosquito Haemagogus sp. Já no meio urbano, a transmissão se dá através do mosquito Aedes aegypti (o mesmo da dengue).
5. Patogênese
As lesões causadas estão relacionadas com o órgão onde ocorre a replicação viral, com consequente necrose celular. As lesões são mais proeminentes no fígado e nos rins, com destruição de grande quantidade de células parenquimatosas.
O fígado mostra-se aumentado de volume, e encontram-se alterações como necrose médio-zonal dos lóbulos hepáticos, esteatose e degeneração eosinofílica dos hepatócitos denotando a lesão hepática devido a apoptose das células.
Os rins apresentam-se aumentados de volume, com edema intersticial e discreto infiltrado inflamatório mononuclear. O epitélio tubular pode apresentar desde degeneração turva até franca necrose devido à coagulação sanguínea.
Além da lesão tecidual provocada pela propagação viral, o processo de coagulação sanguínea intravascular disseminada também pode desempenhar importante papel na fisiopatologia da doença.
6. Manifestações clínicas
Cerca de 85% dos casos da doença apresentam-se como formas clínicas benignas que evoluem para a cura, enquanto 15% desenvolvem quadros dramáticos com mortalidade em torno de 50%.
O período de incubação varia de 3 a 6 dias, e observa-se que a maioria das pessoas infectadas por esse vírus apresenta infecção subclínica. Quando os sintomas ocorrem, aparecem de forma súbita, como febre alta, mal-estar, cefaleia, dor muscular, cansaço e calafrios, podendo também apresentar diarreia e vômito.
A maioria dos pacientes melhora após 4 dias, com recuperação total. No entanto, em aproximadamente 15% dos pacientes, depois desse período de remissão, os sintomas reaparecem evoluindo para uma forma grave da doença. Esses pacientes apresentam febre alta, dor epigástrica, diarreia e vômito, que pode ser hemorrágico, conhecido como vômito negro, além de outras manifestações hemorrágicas como equimoses, epistaxe e gengivorragia.
7. Icterícia
A replicação viral nas células de Kupffer (macrófagos hepáticos) leva à diminuição na taxa de formação de protrombina e à icterícia, entretanto uma resposta inflamatória é ausente ou fraca.
Os pacientes mostram alterações das funções hepáticas devido ao funcionamento inadequado do fígado, além de comprometimento renal, com diminuição do volume urinário que evolui para anúria total seguida de coma. Nos casos graves, 50% dos pacientes evoluem para óbito, e o restante se recupera totalmente sem deixar sequelas.
8. Isolamento e identificação viral
O material de escolha para isolamento viral é o sangue ou soro do paciente, coletado até o 4º dia da doença. A biópsia de fígado durante a doença é contraindicada devido a casos de hemorragia fatal observados em pacientes nos quais esse procedimento foi realizado.
O sangue ou soro podem ser inoculados em culturas de células de animais e em culturas de células de mosquito, camundongos recém-nascidos ou intratoracicamente em mosquitos.
A identificação pode ser feita por testes sorológicos, como teste de neutralização (TN), inibição da hemaglutinação (HI), fixação de complemento (FC), imunofluorescência (IF) e ensaio imunoenzimático (EIA).
9. Pesquisa de anticorpos
A sorologia produz resultados bem definidos quando realizada em pacientes expostos pela primeira vez a um flavivírus. No entanto, quando a pessoa foi exposta anteriormente a outro flavivírus, a reação é rápida e intensa em função da memória imunológica prévia.
Nesse caso, os anticorpos heterólogos são iguais ou mais elevados que os específicos, dificultando a interpretação das reações sorológicas. Podem-se realizar a sorologia pareada empregando teste de neutralização, inibição da hemaglutinação ou fixação do complemento, assim como a pesquisa de anticorpos específicos da classe IgM por imunofluorescência ou ensaio imunoenzimático.
10. Detecção do material genético viral
Para a detecção do ácido nucleico viral no sangue do paciente, pode ser utilizada a reação em cadeia da polimerase associada à reação de transcrição reversa (RT-PCR) convencional ou em tempo real e hibridização em microarranjos (microarray hibridization). A hibridização em microarranjos não é empregada ainda no diagnóstico de rotina.
Santos, Norma Suely de O. Virologia humana. 3. ed. – Rio de Janeiro: Guanabara Koogan, 2015. | Imagens: Popular Science





